

 人类大脑起源于漫长的生命进化过程,其最显著的改变是大脑的认知功能,反映在脑容量的显著扩大和脑结构的高度精细化。人类进化过程中,哪些遗传改变造就了人类大脑是国际科学界长期力图解决的科学问题。
人类大脑起源于漫长的生命进化过程,其最显著的改变是大脑的认知功能,反映在脑容量的显著扩大和脑结构的高度精细化。人类进化过程中,哪些遗传改变造就了人类大脑是国际科学界长期力图解决的科学问题。
所有器官包括大脑的形成都是通过发育过程来实现的。人类独特的脑发育模式源于在进化过程中基因组不断积累的功能性突变。然而,由于物种间存在数以百万计的序列差异,而其中只有少数的关键差异才具有重要的功能效应,如何将基因组中的关键序列差异与脑发育的调控改变之间建立因果联系并解析其中的分子调控机制是颇具挑战的课题。灵长类动物作为生物学和医学研究模型已有近百年的历史。猕猴与人类具有较近的亲缘关系,在人类大脑的起源、发育机制和脑疾病的研究中,猕猴是最理想的动物模型。
哺乳动物包括人类的基因组通常长约2米,折叠在仅有10微米的细胞核中。基因组在细胞核的三维空间中是有序折叠的。这样的有序折叠对发育过程中细胞的增殖和有序分化是至关重要的。全基因组染色质空间构象捕获(简称Hi-C)等最新高通量组学技术的开发为精细解析大脑发育过程中基因组的三维组织方式和分子调控机制提供了强大的工具。在该研究中,研究人员通过学科交叉合作开展了跨物种脑发育3D基因组的研究。首先,利用Hi-C技术构建了中国猕猴胎脑神经发育高峰期的高分辨3D基因组图谱。这是目前包括人类在内的灵长类大脑分辨率最高的3D基因组图谱,达到了1.5kb的分辨率,可以高精度地解析脑发育中基因组的空间组织方式。同时,还解析了猕猴胎脑的转录组图谱、染色质开放区图谱以及染色质锚定蛋白CTCF的分布图谱。综合这些猕猴胎脑的多组学图谱数据,研究人员首次构建了猕猴胎脑发育的染色质精细空间构象,鉴定了包括染色质区室、染色质拓扑结构域(简称TAD)以及染色质环(简称Loop)等不同尺度的染色质构象,以及基因组在大脑发育中发挥重要作用的调控元件(如增强子、启动子等)。
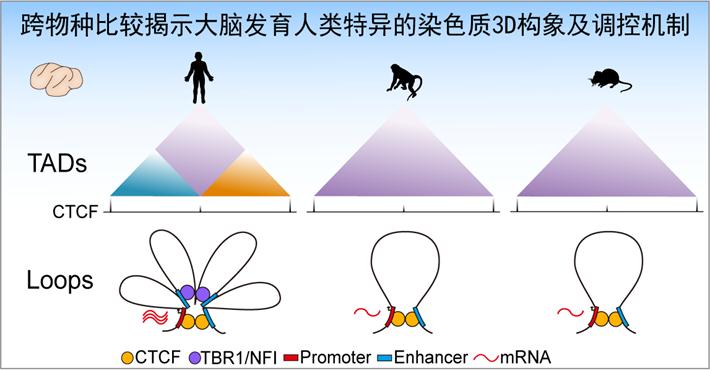
通过与已发表的公共数据整合,研究人员接着进行了跨物种3D基因组的比较(人类、猕猴和小鼠),该研究发现了数量众多的人类特异染色质结构,包括499个人类特异TADs和1266个人类特异Loops。这些人类特异Loops显著富集增强子-增强子互作的调控模式,提示大脑发育在人类祖先中进化出更为精细的转录调控网络。重要的是,通过整合分析人脑发育的单细胞表达谱数据,发现这些人类特异Loops调控的基因在胎脑的SP(subplate)层显著表达,由此推测人类特异Loops对SP层的人类特异发育模式可能发挥重要作用。胎脑SP层是脑发育早期神经环路及神经可塑性形成的重要脑层,在人类进化过程中SP层出现了显著的扩张,其厚度可以达到皮层厚度的4倍左右。但由于在胎儿出生以后,该脑层逐渐消失,人们对其形成机制和功能了解较少。该研究结果首次为SP层在人类特异脑结构的发育和形成中的重要作用提供了证据。
此外,研究人员还发现基因组中很多人类特异突变(包括点突变和结构变异等)位于TAD边界区和Loop锚定区,可能导致在人类大脑发育中产生新的转录因子结合位点,并形成人类特异的染色质高级结构。例如,SP层特异表达的EPHA7基因是大脑发育中神经细胞分化的关键基因之一,该基因的上游存在多个人类特异序列突变,可能导致人类特异增强子的出现和人类特异Loop的形成。通过增强子敲除实验,研究人员证实了EPHA7的人类特异调控网络,干扰其功能会影响神经细胞分化的进程。
这一研究成果首次产生了非人灵长类动物的高精度三维基因组学图谱资源,并利用大脑三维基因组的跨物种多组学分析,发现了人类特异的染色质结构和脑发育调控元件,为阐明人类大脑发育的进化机制提供了新思路和证据。研究论文于2021年1月27日在线发表在国际顶尖学术期刊《细胞》。文章网络链接:3D Genome of macaque fetal brain reveals evolutionary innovations during primate corticogenesis: Cell。罗鑫副研究员(昆明动物所)、刘玉婷(北京大学博士研究生)和党大昌(数学院博士研究生)为论文的共同第一作者,宿兵研究员、李程研究员和张世华研究员为论文的共同通讯作者。北京大学孙育杰教授对成像实验提供了宝贵建议。该研究得到中国科学院、国家自然科学基金委、科技部和云南省相关基金项目的资助。
该项研究工作依托昆明动物研究所承担建设的“模式动物表型与遗传研究国家重大科技基础设施(灵长类)”开展。该设施将对灵长类动物表型与遗传型进行系统研究,连续、快速、精准、标准化、规模化和自动化地获取信息与分析,客观描述、深入解析生命现象变化中的表型与内在的遗传关系,对解码生命,普惠健康具有潜在重要意义。
